Table of Contents
ToggleLes enjeux de la recherche
L’étude du microbiote intestinal est récemment devenue centrale pour la recherche médicale. S’il est probable qu’il constitue un biomarqueur qui reflète différents états de santé, il est également important d’appréhender l’aspect symbiotique qui existe entre ce microbiote et l’organisme. Ainsi, si certaines maladies sont secondaires à une dysbiose, il semble évident que cette dernière peut être causée par certains évènements de santé. Ces relations bidirectionnelles, pour l’heure à peine décrites, doivent continuer à être explorées afin de pouvoir mieux établir le sens des liens qui existent entre dysbiose et maladies.
Par ailleurs, le microbiote intestinal n’est pas seulement bactérien : il contient aussi des champignons et des virus. L’étude des interactions normales ou dysfonctionnelles qui existent entre eux est un champ d’investigation encore récent car complexe à explorer. D’autre part, les interactions entre les différents microbiotes de l’organisme (bouche, fosses nasales, intestin, peau…) pourraient également apporter des informations précieuses sur la façon dont ils se constituent ou évoluent.
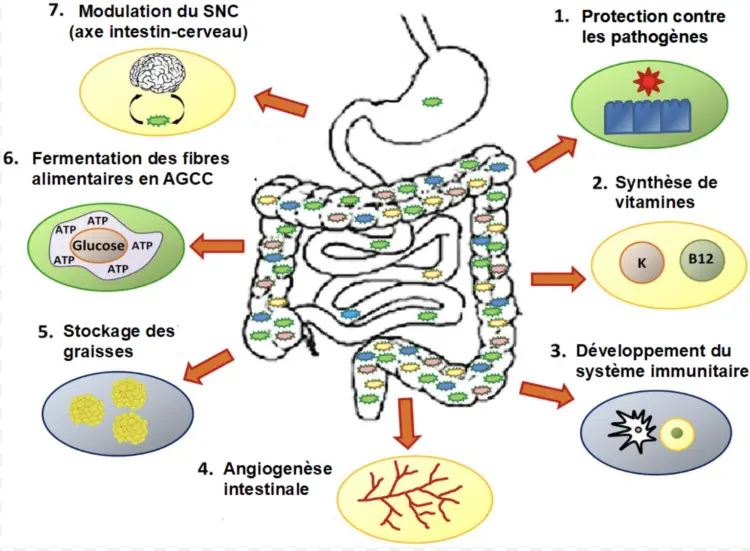
Une partie des études en cours se concentre en outre spécifiquement sur les métabolites produits par le microbiote, car ils représentent un vecteur important de ses effets sur l’hôte. En effet, les déséquilibres microbiens (à l’origine et/ou secondaires à une maladie) peuvent se traduire par des concentrations inhabituelles de certains de ces composés, avec des conséquences sur la santé. Les techniques d’analyse globale des métabolites (la métabolomique) sont de plus en plus utilisées pour étudier ces aspects. Les découvertes réalisées dans ce domaine ouvrent la voie à une nouvelle approche thérapeutique : celle des postbiotiques, qui consiste à apporter directement à l’organisme des métabolites bénéfiques, habituellement produits par les micro-organismes intestinaux.
Maladies intestinales : un lien évident
Les maladies inflammatoires chroniques de l’intestin (MICI), comme la maladie de Crohn et la rectocolite hémorragique, sont liées à une activation inappropriée du système immunitaire dans l’intestin. Derrière leur survenue se cachent des facteurs génétiques et environnementaux (alimentation, âge…). Le rôle du microbiote a été suspecté devant l’amélioration des symptômes de patients sous traitement antibiotique, ou encore en raison de la disparition de lésions inflammatoires intestinales chez des personnes dont la paroi intestinale n’est plus au contact des fèces (suite à la mise en place d’une dérivation fécale). Ceci s’explique probablement par le rôle des bactéries intestinales et leurs métabolites dans l’équilibre de la réponse immunitaire locale.
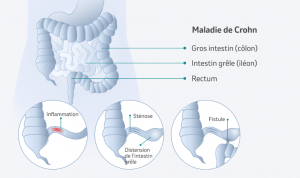
Des dysbioses associées aux MICI ont été décrites. Elles sont caractérisées par un déficit en certaines bactéries, comme Faecalibacterium prausnitzii ou d’autres espèces du groupe Clostridium, ainsi que par une augmentation de la population d’autres bactéries pro-inflammatoires comme les entérobactériesoules bactéries du genre Fusobacterium. On pense que ces déséquilibres sont à la fois une cause et une conséquence de la maladie : la dysbiose apparaîtrait sous l’influence de facteurs génétiques et environnementaux, mais jouerait elle-même un rôle dans le démarrage, le maintien ou la sévérité de l’inflammation, engendrant un cercle vicieux. Le rôle des métabolites bactériens dans ces mécanismes est aussi suspecté.
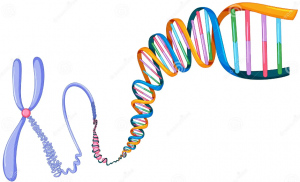 Parmi les dizaines de gènes de prédisposition aux MICI aujourd’hui identifiés, certains jouent un rôle déterminant vis-à-vis du microbiote. C’est par exemple le cas du gène NOD2, dont les variations sont celles qui ont le plus de poids dans le risque de survenue de la maladie de Crohn en occident. Or ce gène code pour un récepteur de l’immunité innée, chargé de détecter un composant de la paroi bactérienne. Muté, il ne peut plus jouer ce rôle et favoriser le maintien de la barrière intestinale. Autre exemple, celui des polymorphismes qui affectent le gène CARD9, également impliqué dans la reconnaissance des micro-organismes par l’immunité innée. Son dysfonctionnement favorise le déséquilibre du microbiote et l’instauration d’une inflammation au niveau local.
Parmi les dizaines de gènes de prédisposition aux MICI aujourd’hui identifiés, certains jouent un rôle déterminant vis-à-vis du microbiote. C’est par exemple le cas du gène NOD2, dont les variations sont celles qui ont le plus de poids dans le risque de survenue de la maladie de Crohn en occident. Or ce gène code pour un récepteur de l’immunité innée, chargé de détecter un composant de la paroi bactérienne. Muté, il ne peut plus jouer ce rôle et favoriser le maintien de la barrière intestinale. Autre exemple, celui des polymorphismes qui affectent le gène CARD9, également impliqué dans la reconnaissance des micro-organismes par l’immunité innée. Son dysfonctionnement favorise le déséquilibre du microbiote et l’instauration d’une inflammation au niveau local.
Transplantation fécale et probiotiques : deux pistes thérapeutiques à étude
Ainsi, le microbiote constitue une cible thérapeutique de choix dans ces maladies inflammatoires de l’intestin. La prise en charge de ces maladies pourrait donc évoluer vers l’association de traitements médicamenteux tels que ceux qui actuellement utilisés et d’approches qui agiront sur le microbiote.
 Une approche prometteuse est celle de la transplantation fécale : il s’agit d’extraire un échantillon de microbiote normal à partir des fèces de donneurs sains et de l’instiller à une personne malade. Le succès de cette approche dépend de l’importance du rôle de la dysbiose dans la pathogénie de la maladie : ce traitement est par exemple très efficace – et désormais utilisé en routine – pour traiter la diarrhée des patients qui souffrent d’une infection récidivante à Clostridioides difficile. Les résultats des essais conduits dans le traitement des MICI sont également encourageantes. En revanche, l’efficacité de la transplantation fécale reste controversée dans la prise en charge du syndrome de l’intestin irritable.
Une approche prometteuse est celle de la transplantation fécale : il s’agit d’extraire un échantillon de microbiote normal à partir des fèces de donneurs sains et de l’instiller à une personne malade. Le succès de cette approche dépend de l’importance du rôle de la dysbiose dans la pathogénie de la maladie : ce traitement est par exemple très efficace – et désormais utilisé en routine – pour traiter la diarrhée des patients qui souffrent d’une infection récidivante à Clostridioides difficile. Les résultats des essais conduits dans le traitement des MICI sont également encourageantes. En revanche, l’efficacité de la transplantation fécale reste controversée dans la prise en charge du syndrome de l’intestin irritable.
Il est aussi possible d’agir sur la composition du microbiote intestinal de patient grâce aux probiotiques. Toutefois, les essais cliniques qui ont évalué le bénéfice de probiotiques « conventionnels », issus de produits fermentés, n’ont pas été concluants. La recherche s’oriente donc vers l’utilisation de probiotiques « de nouvelle génération », identifiés de manière rationnelle dans le microbiote intestinal pour leurs effets biologiques. On peut espérer que ces bactéries actuellement à l’étude, dont l’intestin est l’habitat naturel, auront des effets plus puissants. Certaines équipes essayent aussi de créer des probiotiques génétiquement modifiés,dotés de propriétés supplémentaires telle que la capacité à sécréter des immunomodulateurs.
Enfin, des travaux qui visent à caractériser et utiliser cliniquement des métabolites bactériens d’intérêt (postbiotiques) sont en cours.
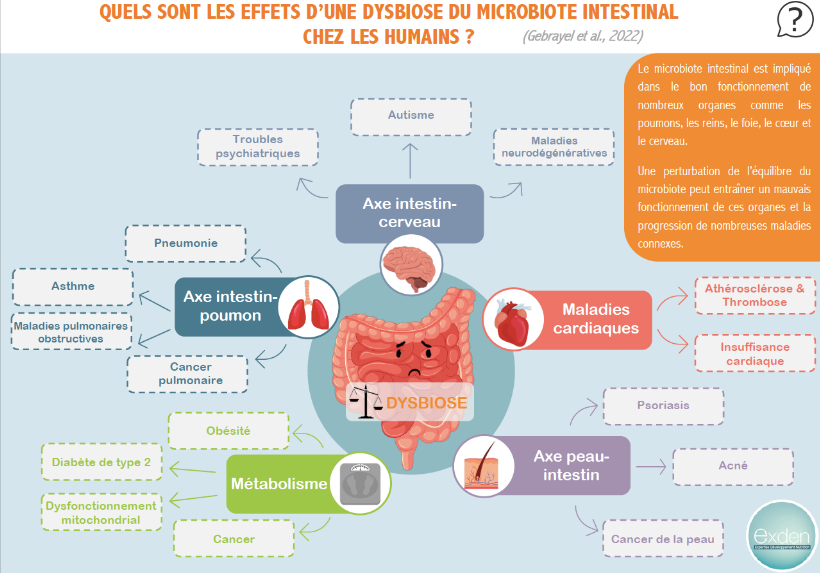
Dysbiose, métabolisme et maladies cardiovasculaires
 Les maladies cardio- et cérébrovasculaires (athérosclérose, hypertension, AVC…) et cardiométaboliques (diabète, obésité) ont une origine multifactorielle, à la fois génétique, nutritionnelle et environnementale. La part respective de chacun de ces facteurs est variable d’un individu à l’autre et les mécanismes moléculaires sous-jacents à chacun d’entre eux restent à décrire précisément. Cependant, il apparaît de plus en plus clairement que le microbiote intestinal joue un rôle dans leur genèse. Il est par exemple décrit que l’implantation d’un microbiote qui provient d’une souris obèse chez une souris axénique provoque une prise de poids importante et rapide chez cette dernière. On sait aussi que la prise d’antibiotiques au long cours peut avoir une incidence sur le risque de développer une maladie cardiovasculaire.
Les maladies cardio- et cérébrovasculaires (athérosclérose, hypertension, AVC…) et cardiométaboliques (diabète, obésité) ont une origine multifactorielle, à la fois génétique, nutritionnelle et environnementale. La part respective de chacun de ces facteurs est variable d’un individu à l’autre et les mécanismes moléculaires sous-jacents à chacun d’entre eux restent à décrire précisément. Cependant, il apparaît de plus en plus clairement que le microbiote intestinal joue un rôle dans leur genèse. Il est par exemple décrit que l’implantation d’un microbiote qui provient d’une souris obèse chez une souris axénique provoque une prise de poids importante et rapide chez cette dernière. On sait aussi que la prise d’antibiotiques au long cours peut avoir une incidence sur le risque de développer une maladie cardiovasculaire.
 Plusieurs mécanismes pourraient être à l’origine de ces relations : dans le diabète ou l’obésité, il existe une inflammation chronique, favorisée par l’augmentation des graisses dans l’alimentation. Ces dernières augmentent la proportion des bactéries à Gram négatif dans l’intestin et donc le taux local de LPS inflammatoire (voir plus haut Microbiote et inflammation). Le LPS est ensuite capable de passer dans la circulation sanguine, dans le foie, les tissus adipeux, musculaires… où il favorise l’installation d’une inflammation chronique à bas bruit. Celle-ci va à son tour favoriser l’apparition d’une insulinorésistance, préalable au diabète et à l’obésité.
Plusieurs mécanismes pourraient être à l’origine de ces relations : dans le diabète ou l’obésité, il existe une inflammation chronique, favorisée par l’augmentation des graisses dans l’alimentation. Ces dernières augmentent la proportion des bactéries à Gram négatif dans l’intestin et donc le taux local de LPS inflammatoire (voir plus haut Microbiote et inflammation). Le LPS est ensuite capable de passer dans la circulation sanguine, dans le foie, les tissus adipeux, musculaires… où il favorise l’installation d’une inflammation chronique à bas bruit. Celle-ci va à son tour favoriser l’apparition d’une insulinorésistance, préalable au diabète et à l’obésité.
D’autres mécanismes qui impliquent le microbiote entrent probablement aussi en jeu : l’augmentation de la perméabilité de la paroi intestinale pourrait laisser passer des bactéries entières. Leur implantation durable au niveau des tissus adipeux, musculaires et hépatiques participerait alors le maintien de l’inflammation in situ.
 Enfin, certains métabolites bactériens auraient un rôle déterminant dans le développement de maladies cardiométaboliques comme le diabète de type 2, l’athérosclérose ou l’hypertension artérielle. Les données les plus probantes concernent notamment la triméthylamine : ce déchet produit par le microbiote peut passer dans la circulation sanguine et être oxydé par le foie en triméthylamine-N-oxyde, une substance qui favorise la formation de plaques d’athérome. D’autres composés comme le benzoate, l’hippurate ou le crésol modifient eux aussi le risque cardiovasculaire.
Enfin, certains métabolites bactériens auraient un rôle déterminant dans le développement de maladies cardiométaboliques comme le diabète de type 2, l’athérosclérose ou l’hypertension artérielle. Les données les plus probantes concernent notamment la triméthylamine : ce déchet produit par le microbiote peut passer dans la circulation sanguine et être oxydé par le foie en triméthylamine-N-oxyde, une substance qui favorise la formation de plaques d’athérome. D’autres composés comme le benzoate, l’hippurate ou le crésol modifient eux aussi le risque cardiovasculaire.
Vers des traitements individualisés
L’idée est aujourd’hui de développer des stratégies personnalisées, dans lesquelles l’apport de prébiotiques, probiotiques, symbiotiques ou postbiotiques serait adapté aux spécificités individuelles du patient. A plus long terme, le même type d’approche pourrait être développé afin de prévenir la survenue de ces maladies.
Par ailleurs, des essais de transplantation fécale ont été conduits chez des patients obèses ou atteints de syndrome métaboliques : certains paramètres biologiques ont évolué favorablement mais l’ampleur de l’effet reste pour l’heure très modeste. Les études se poursuivent.